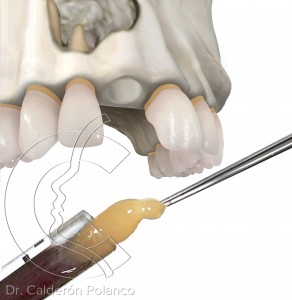
El L-PRF (Leukocyte – Platelet Rich Fibrin) o «Fibrina Rica en Plaquetas y Leucocitos» es un preparado autólogo (derivado de una extracción de sangre del propio paciente) que se obtiene en el mismo momento de la cirugía).
Contiene una malla de fibrina con un alto contenido en plaquetas y leucocitos, que libera factores de crecimiento que estimulan y aceleran la curación de los tejidos, regulando la inflamación e infección post-quirúrgica.
El L-PRF libera factores de crecimiento, de forma lenta y mantenida, durante al menos 7 días, que promueven la angiogénesis (formación de vasos sanguíneos), fundamental para la cicatrización y la formación de tejido.
La malla de fibrina actúa, además, como un andamio sobre el que van creciendo las células endoteliales, encargadas de generar estos neovasos sanguineos.
Además, estimula el crecimiento otros tipos celulares, consiguiendo formar tejido óseo y encía en un tiempo mucho menor.
La presencia de leucocitos en la malla de fibrina regulan la inflamación y la infección post operatoria, mejorando la recuperación post-operatoria del paciente.
El uso de concentrados de plaquetas en Cirugía Oral y Maxilofacial ha sido ampliamente estudiado en los últimos año, existiendo numerosos protocolos, la mayoría conocidos como “Plasma Rico en Plaquetas” que no han logrado demostrar resultados concluyentes.
Una de las principales diferencias del L-PRF con los diferentes protocolos de Plasma Rico en Plaquetas es que el procesamiento de la sangre en el L-PRF es completamente natural y no se utilizan anticoagulantes durante la obtención de la sangre. Tampoco se utilizan aditivos químicos (cloruro de calcio) ni trombina de vaca para la activación de las plaquetas y la polimerización de la fibrina. De hecho, el L-PRF puede ser considerado como un coágulo sanguíneo natural optimizado.
A diferencia del resto de preparados, que liberan factores de crecimiento sólo durante los 3 primeros días, el L-PRF lo hace durante 7 días.
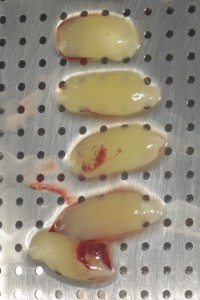

El L-PRF se obtiene por un procedimiento sencillo:
En el mismo momento de la cirugía se extraen unos tubos de 9 ml de sangre del propio paciente, como si fuera un análisis de sangre convencional.
Estos tubos se introducen en una centrífuga (IntraSpin) durante 12 minutos, con lo que conseguimos separar la muestra de sangre en 3 capas: en la base del tubo quedan los glóbulos rojos, en la parte superior un sobrenadante de plasma celular y, entre ambas, un coágulo de fibrina, que es el que finalmente se utiliza.
No es necesario el pipeteado, mezclado, calentamiento o incorporación de aditivos.
Cada componente del Sistema IntraSpin ha sido específicamente diseñado en cumplimiento de la legislación médica y cuenta con la aprobación de la FDA para la fabricación de fibrina rica en plaquetas. El uso de los componentes de IntraSpinTM System asegura la biocompatibilidad y el correcto resultado clínico.
Incluyen pero no se limitan a:
* Los casos clínicos incluyen fotografías intraoperatorias que pueden dañar su sensibilidad.
Haga click en el título para ver las imágenes.
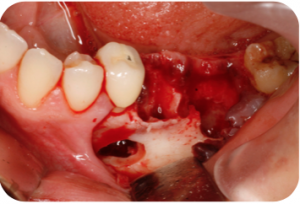
Caso 1 – Defecto post-extracción.
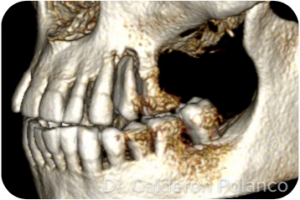
Caso 2 – Atrofia maxilar
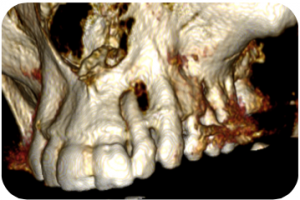
Caso 3 – Quiste en premaxila.
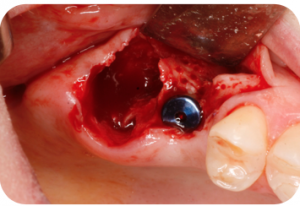
Caso 4 – Defecto Tuberosidad maxilar.
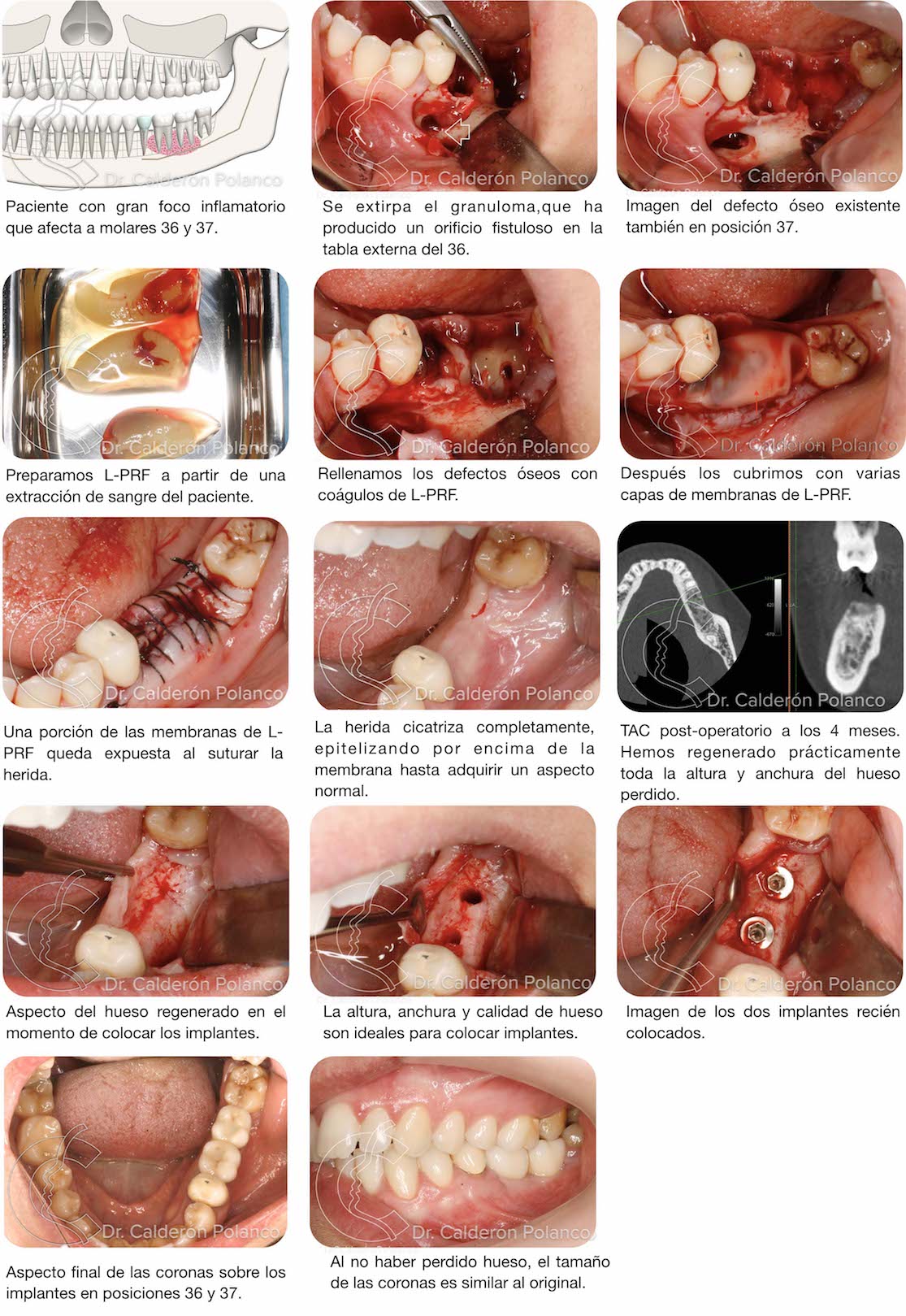
Caso 1: Defecto post-extraccion mandibular.
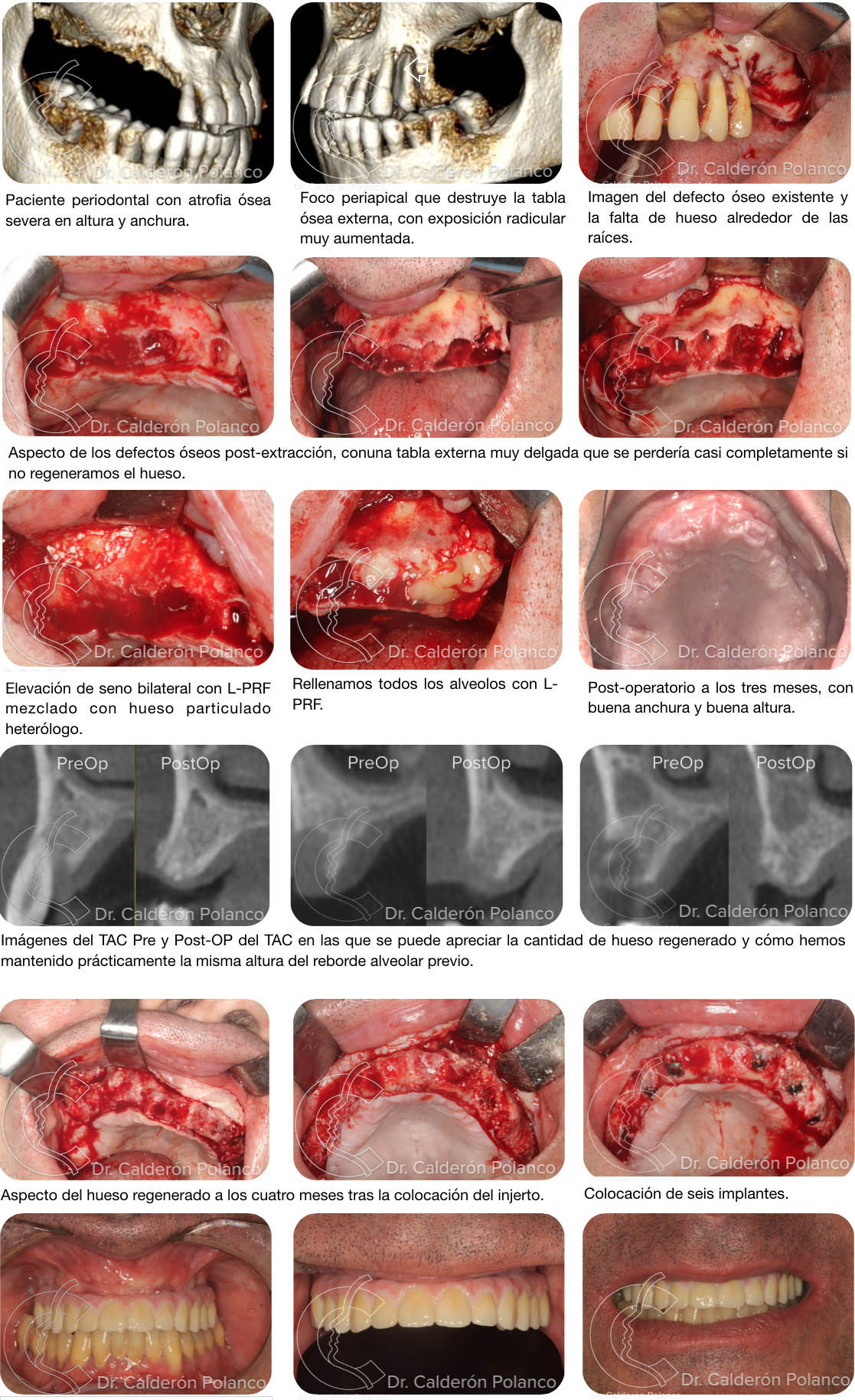
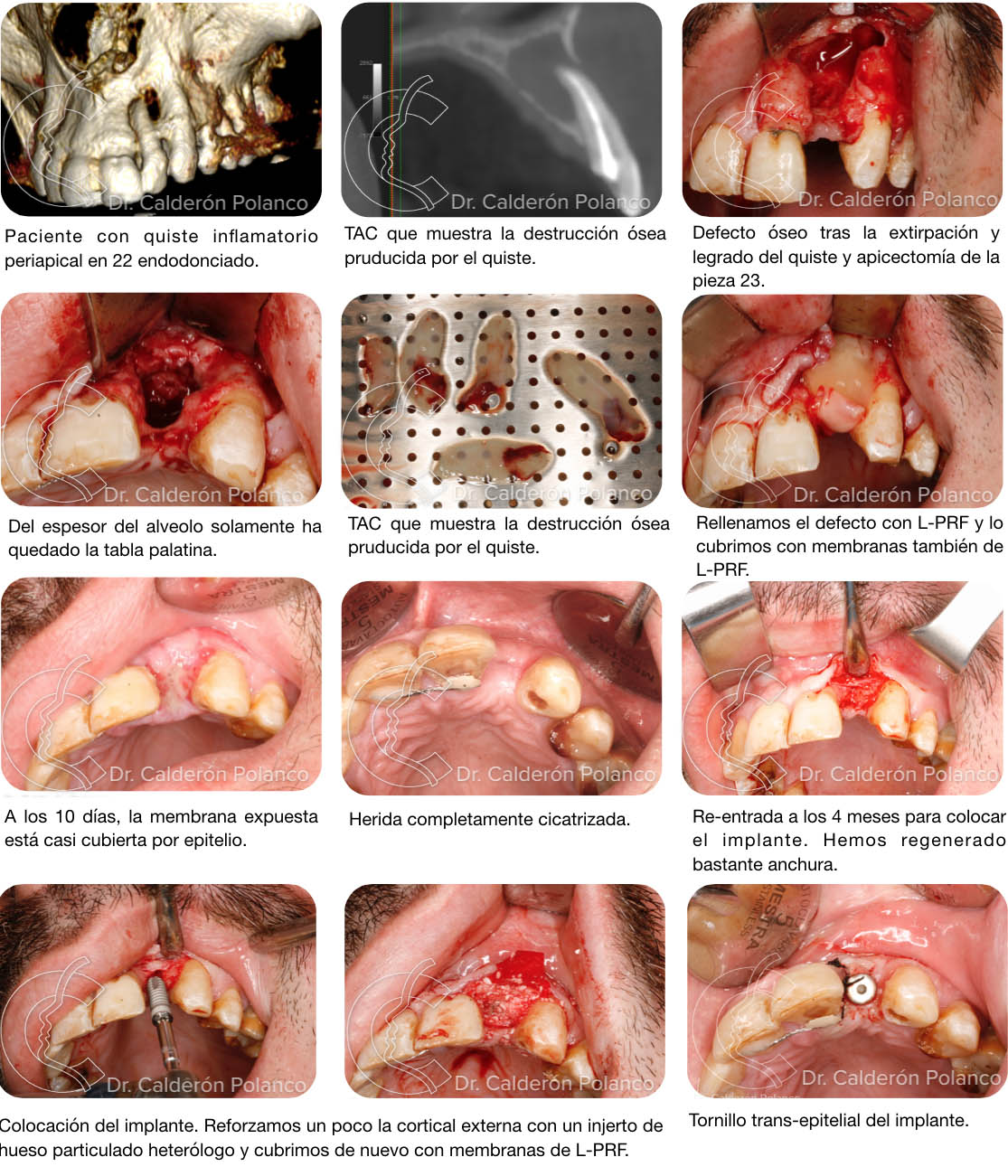
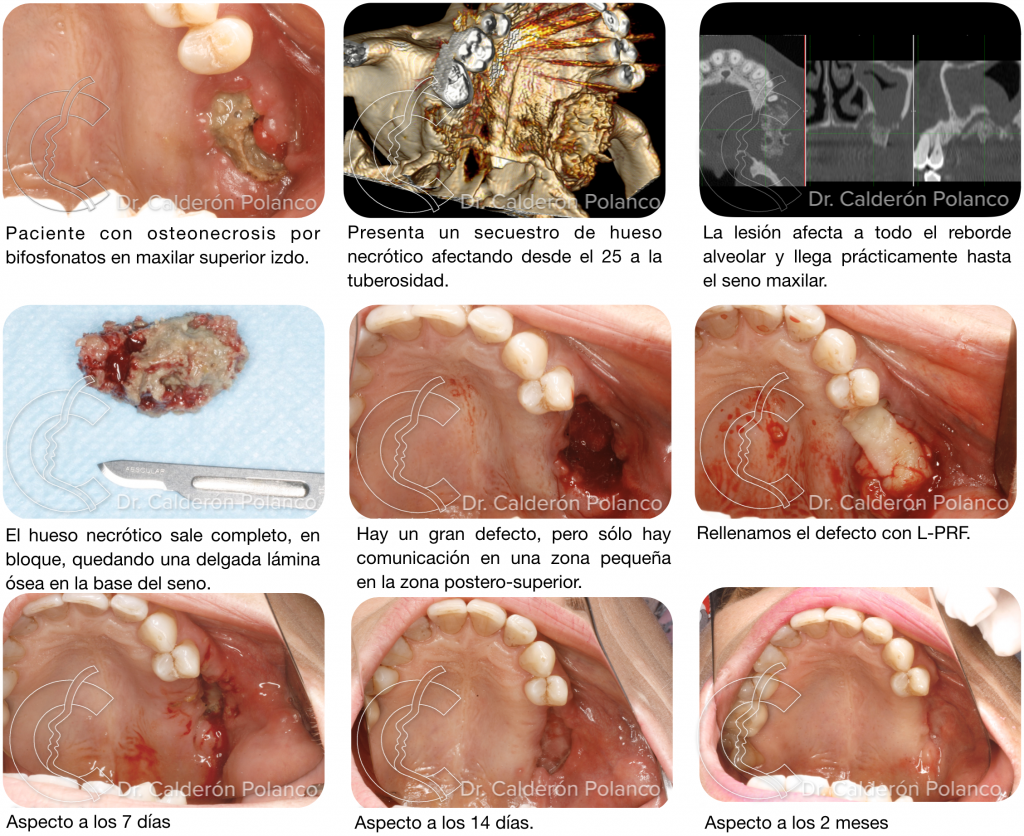
Caso 4: Defecto Tuberosidad maxilar.
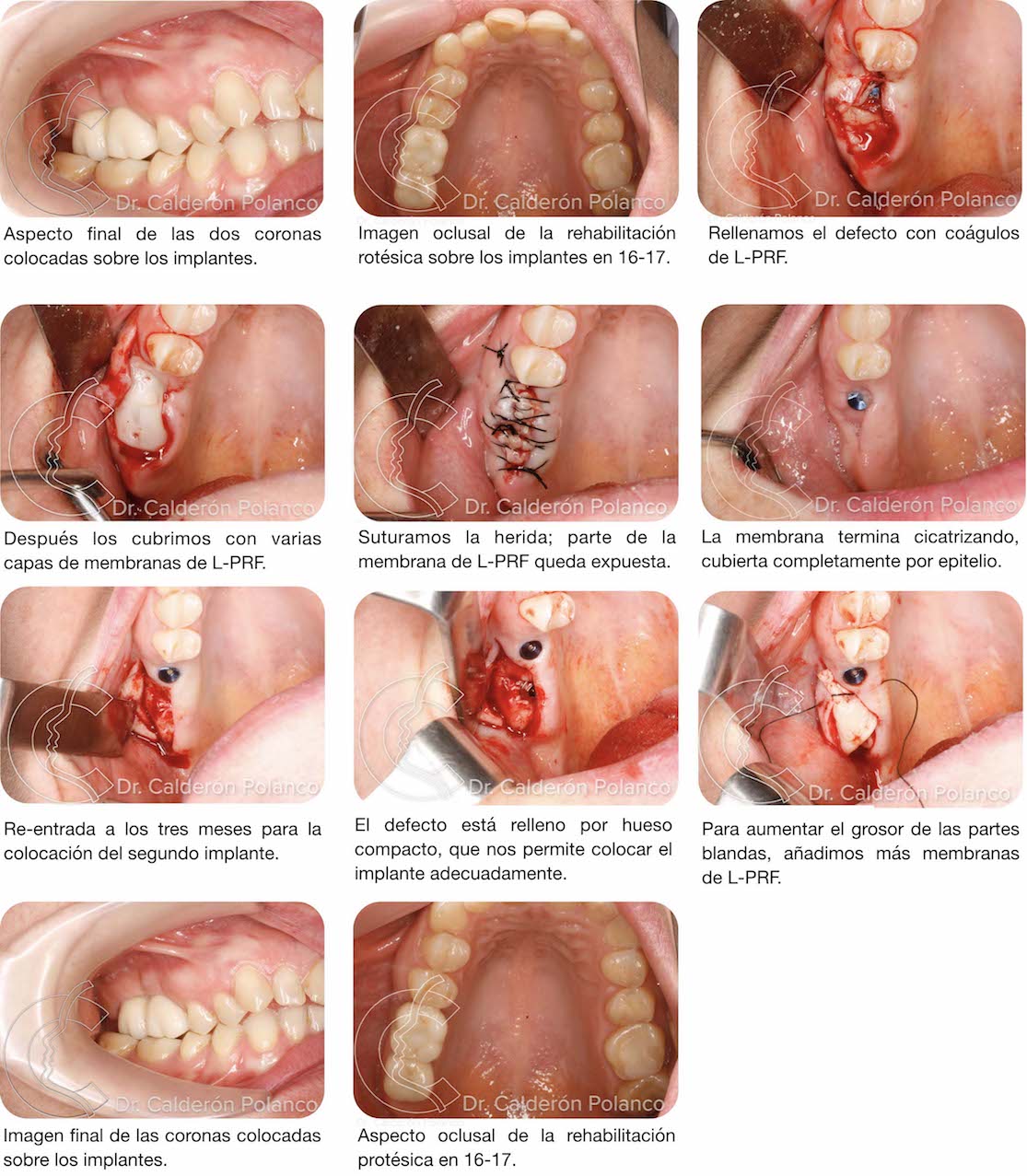
* Los casos clínicos incluyen fotografías intraoperatorias que pueden dañar su sensibilidad.
Haga click en el título para ver las imágenes.
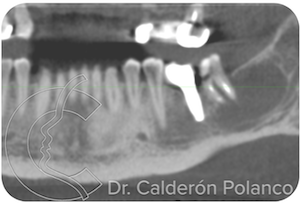
Caso 5 – Quiste en ángulo mandibular.
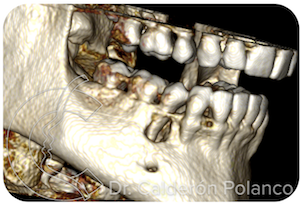
Caso 6 – Quiste inflamatorio mandibular.
Caso 7 – Quiste mandibular.
Caso 8 – Quiste asociado a cordal incluido.
Caso 5: Quiste en ángulo mandibular.
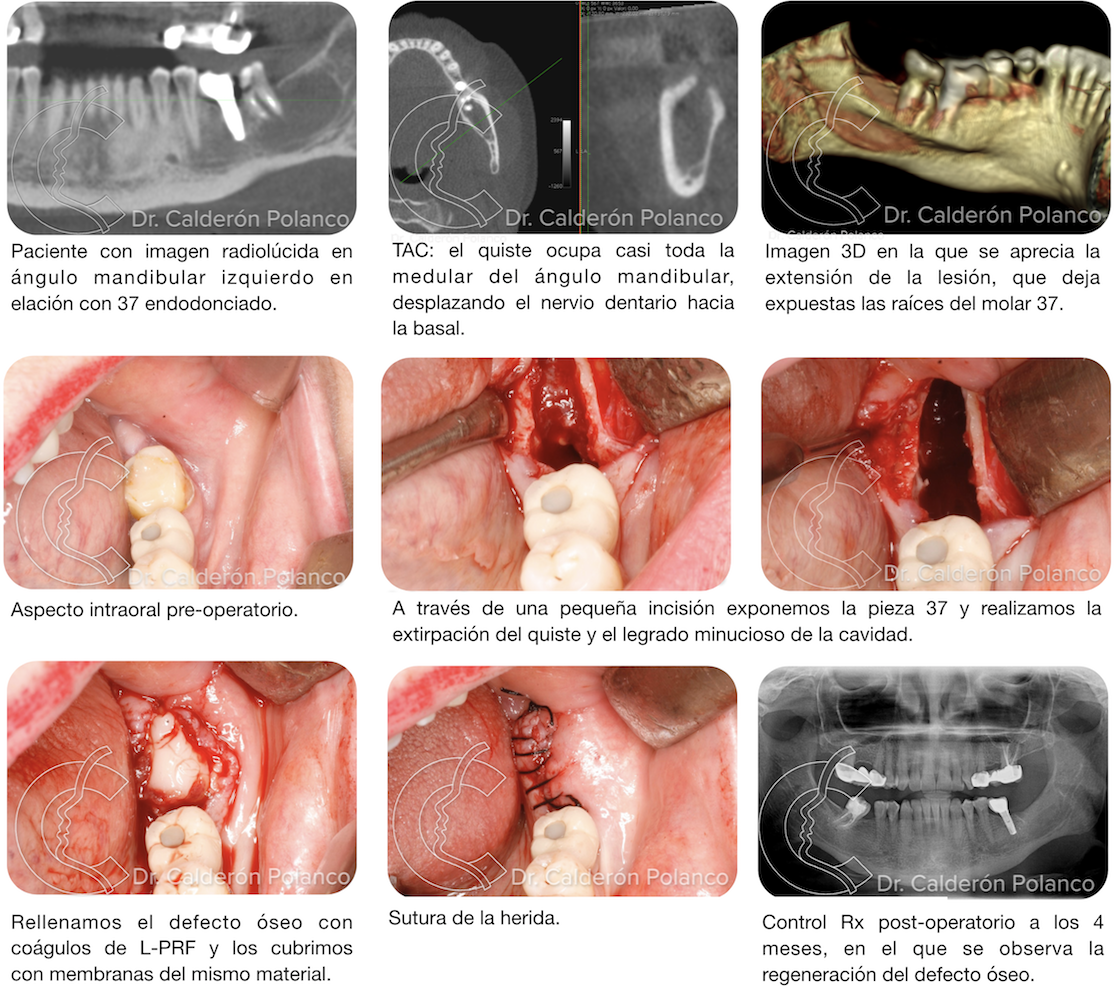
Caso 6: Quiste inflamatorio mandibular.
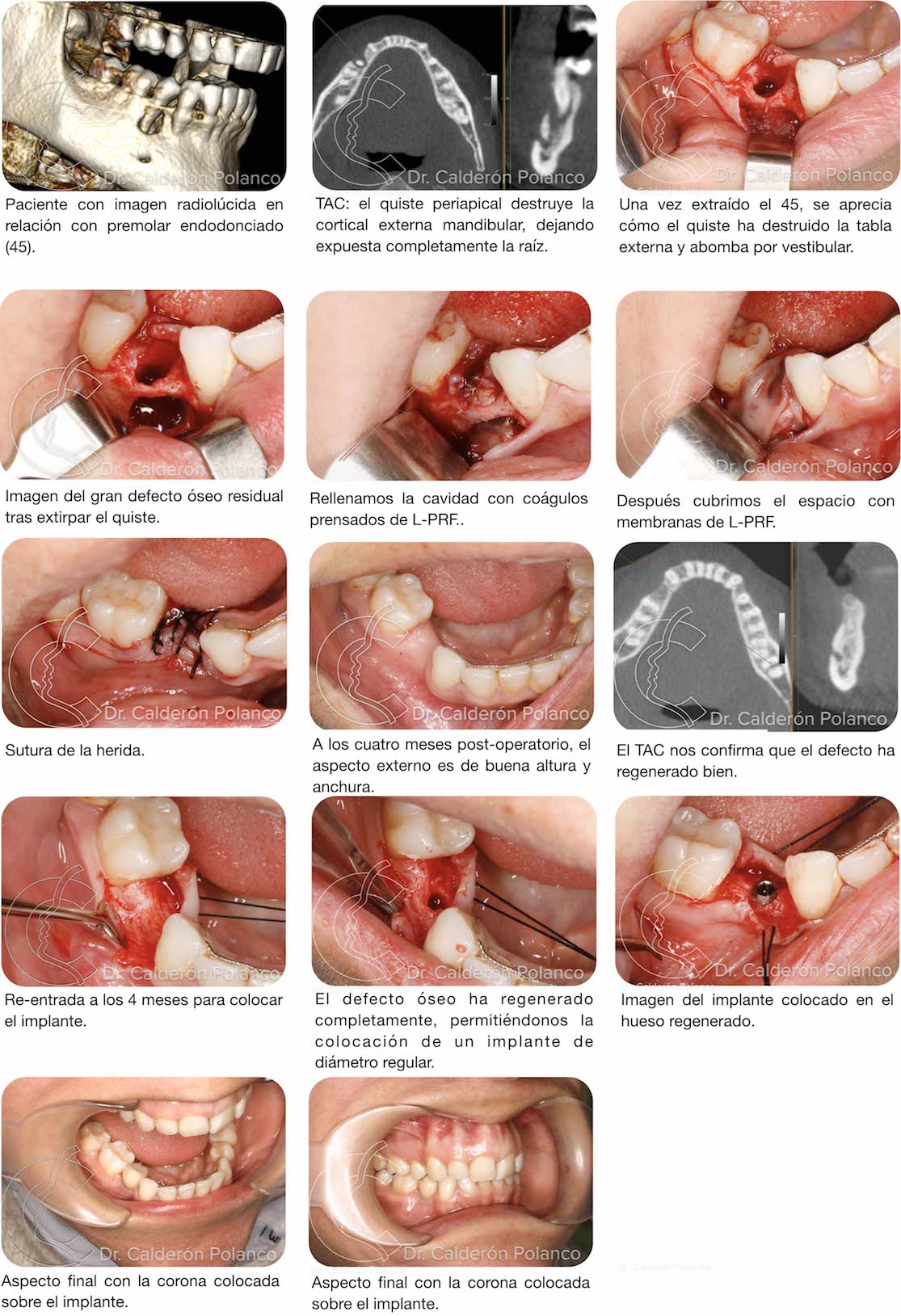
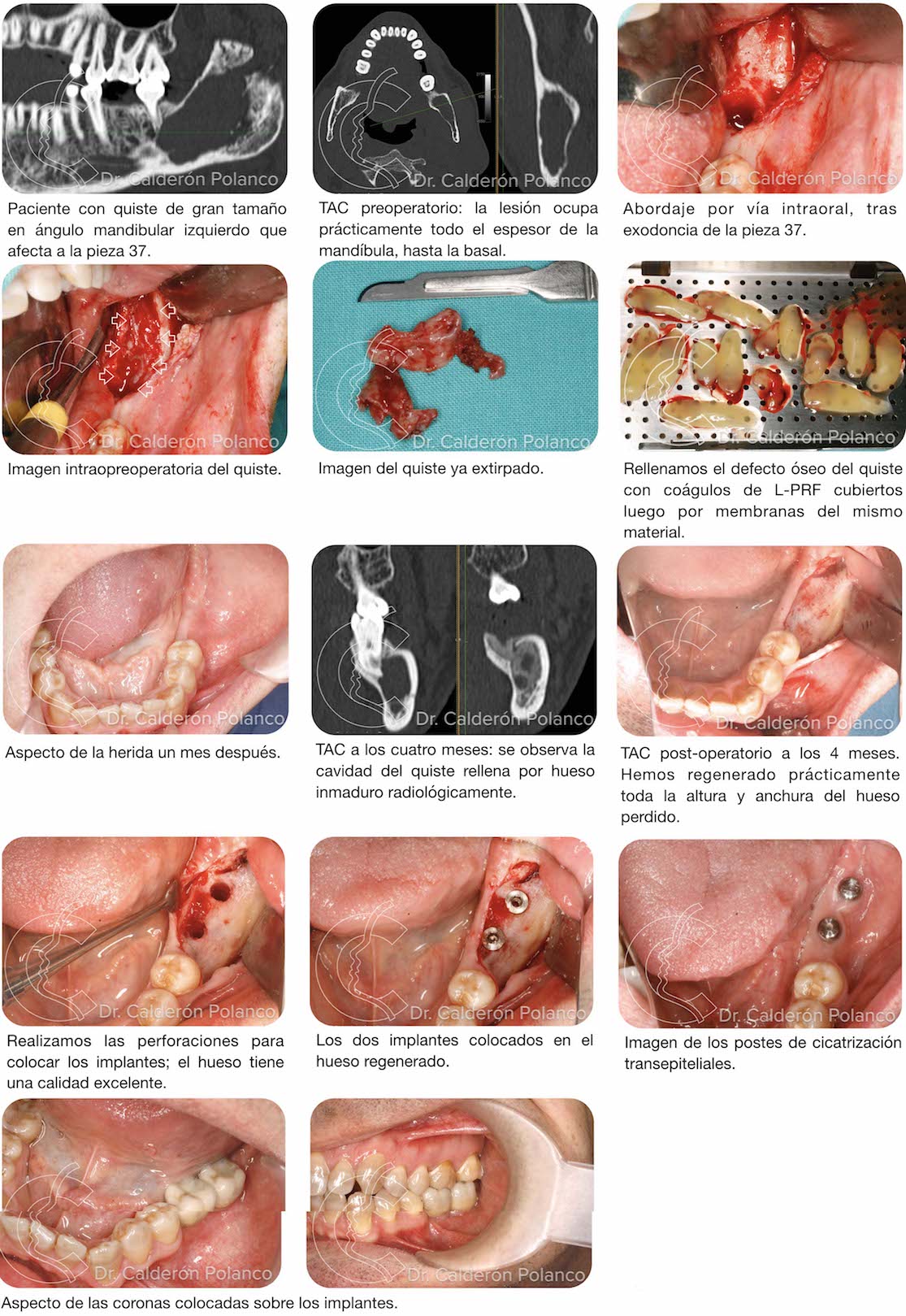
Caso 8: Quiste asociado a cordal incluido.
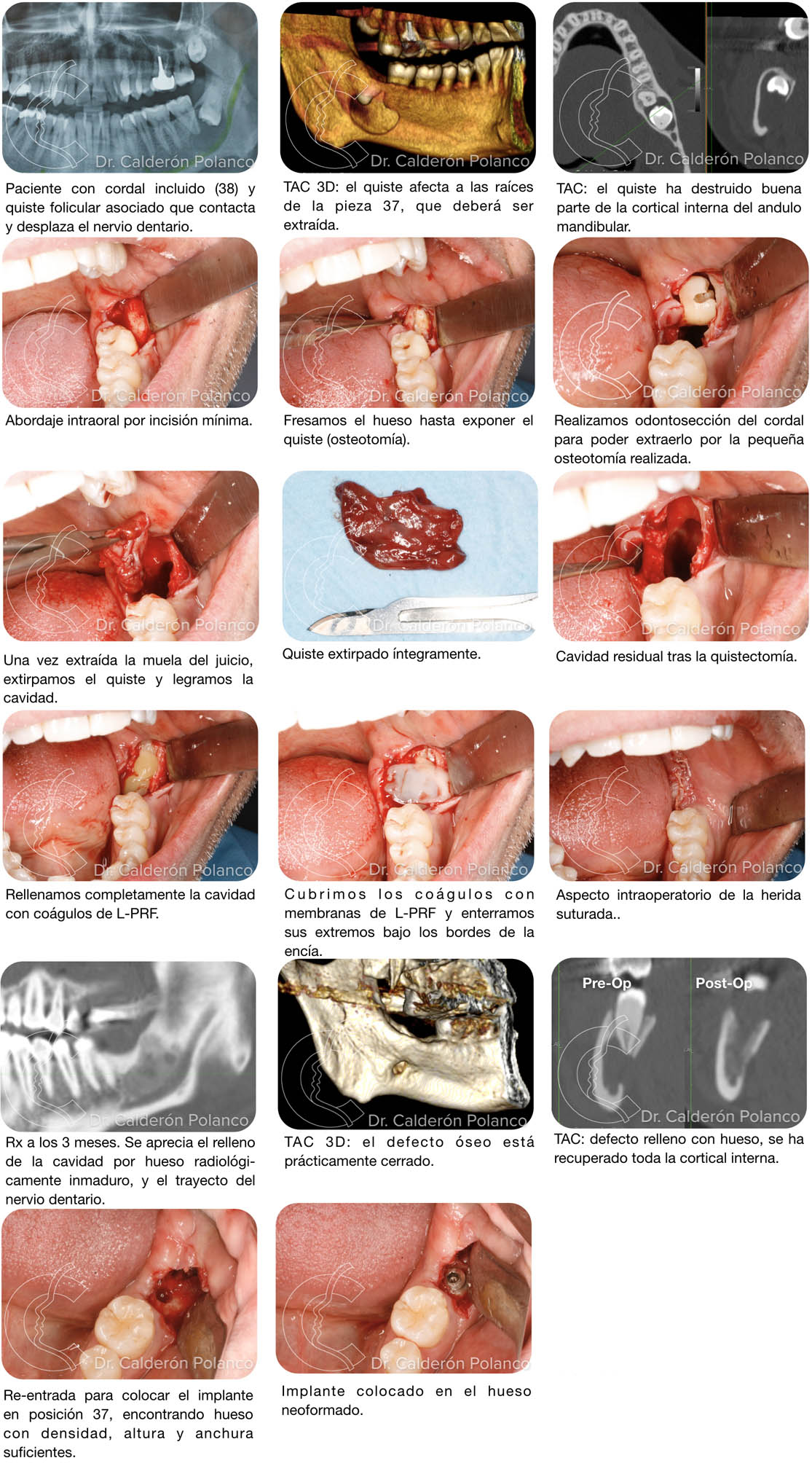
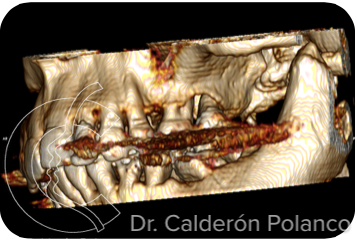
Caso 9 – Defecto post-extracción en maxilar superior.
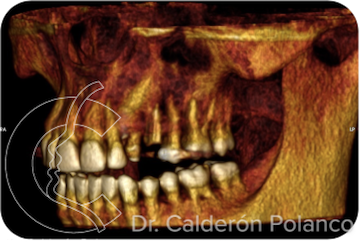
Caso 10 – Implante tras canino incluido
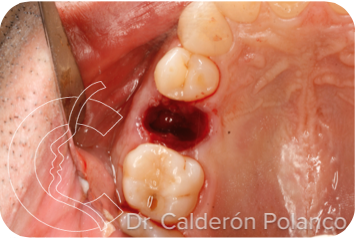
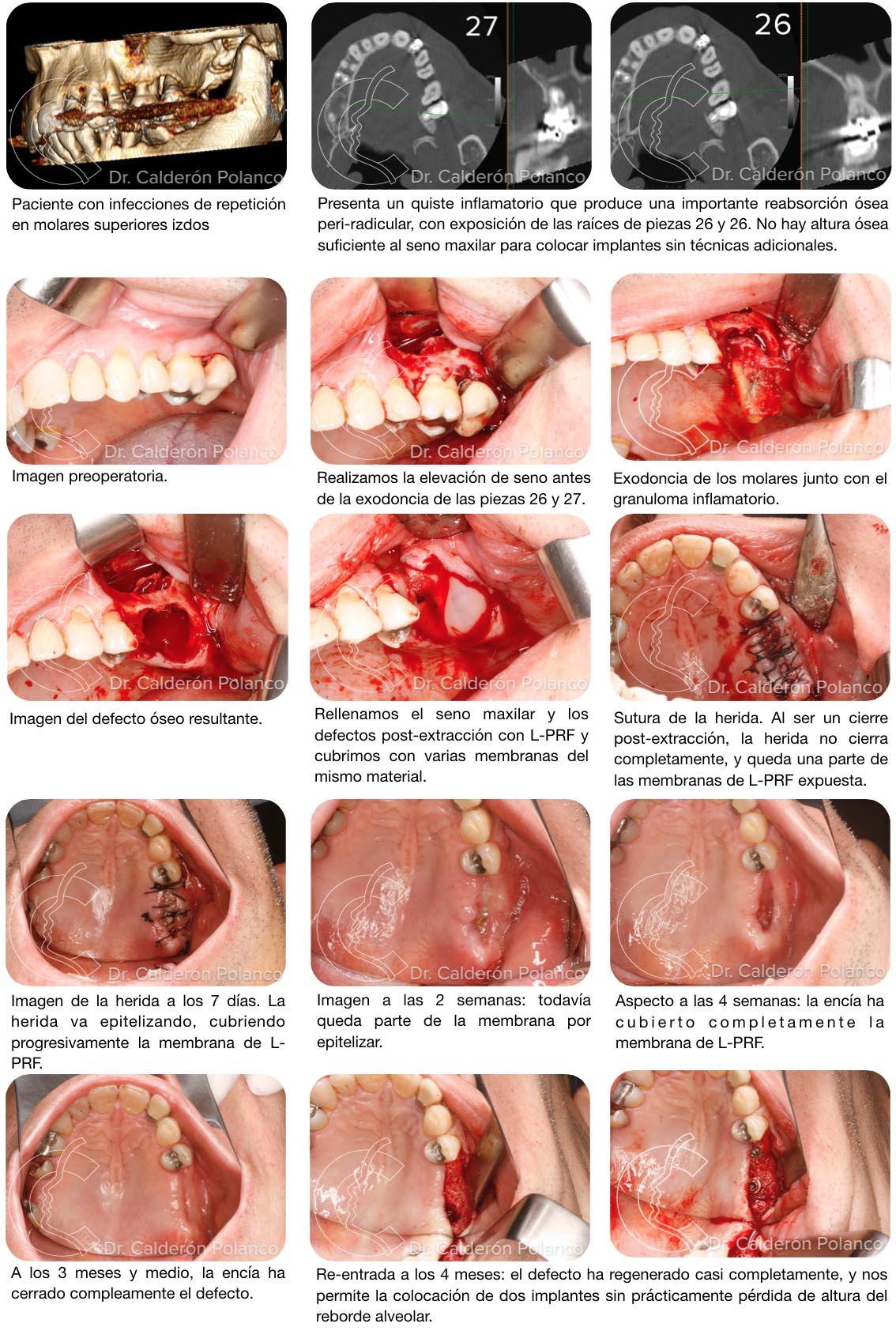
Caso 11 – Defecto post-extracción en premolares.
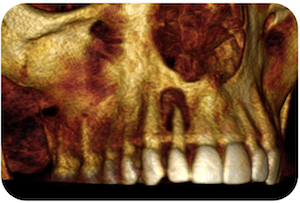
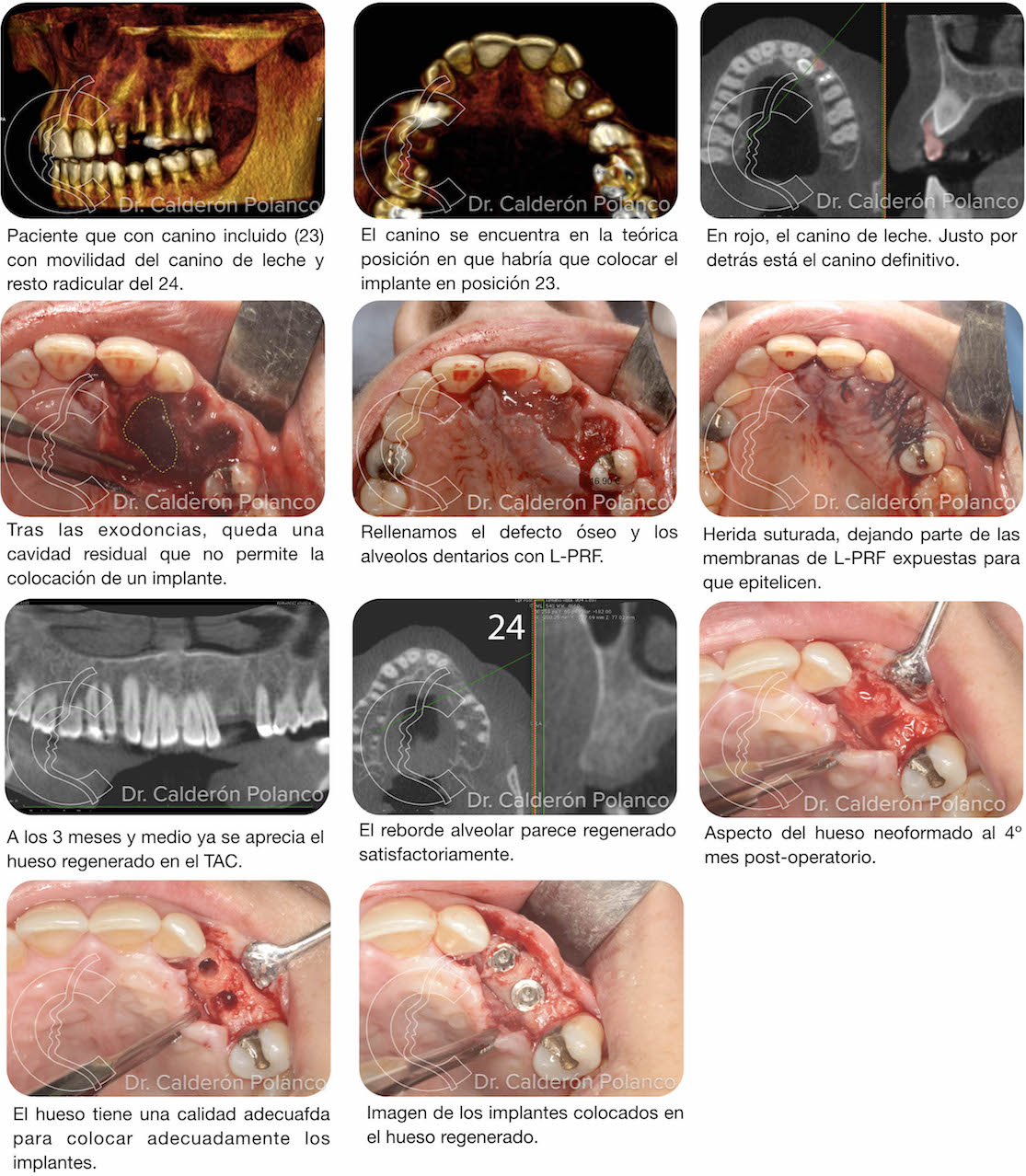
Caso 12 – Quiste en incisivo lateral
Caso 9: Defecto post-extracción en maxilar superior
Caso 10: Implante tras exodoncia de canino incluido.
Caso 11: Defecto post-extracción en premolares.
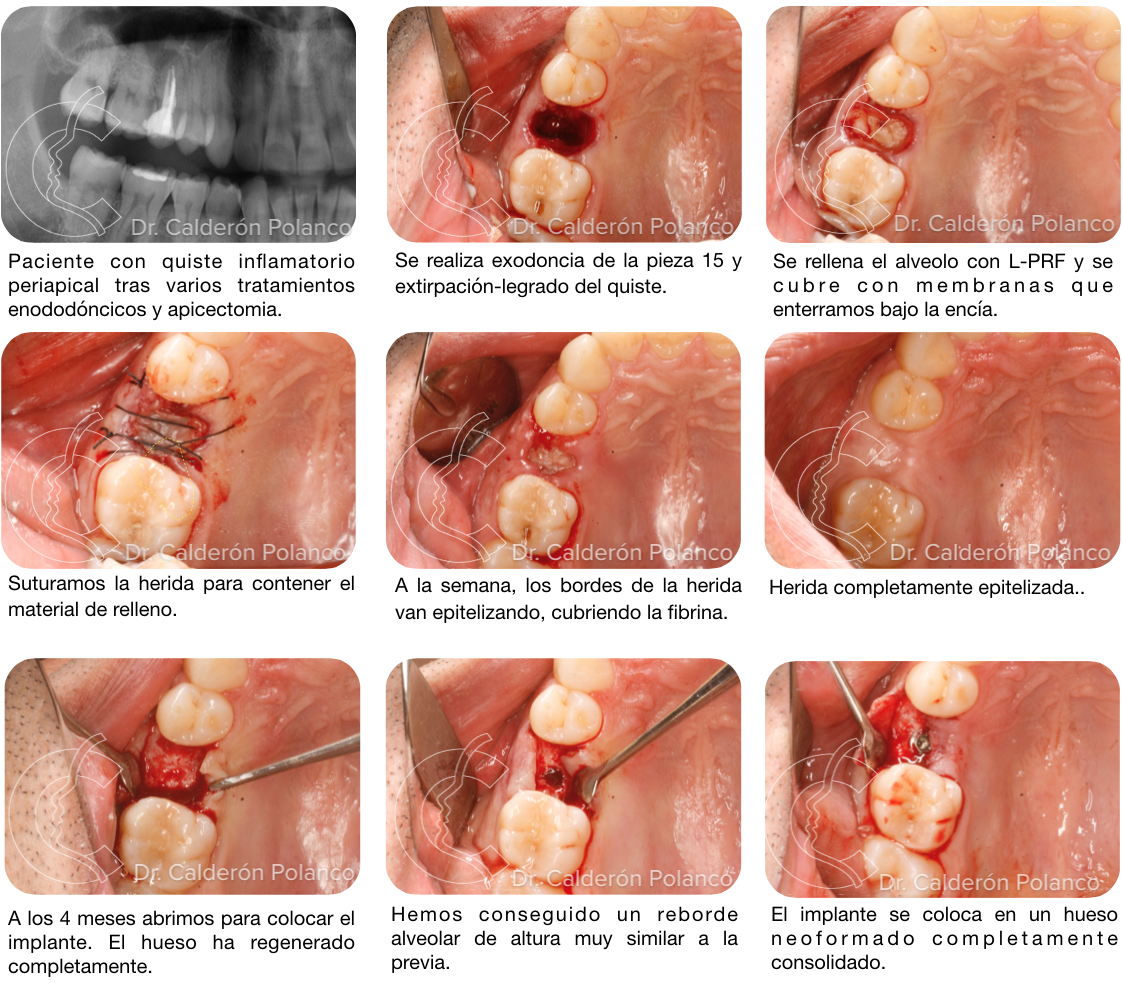
Caso 12: Quiste en incisivo lateral.
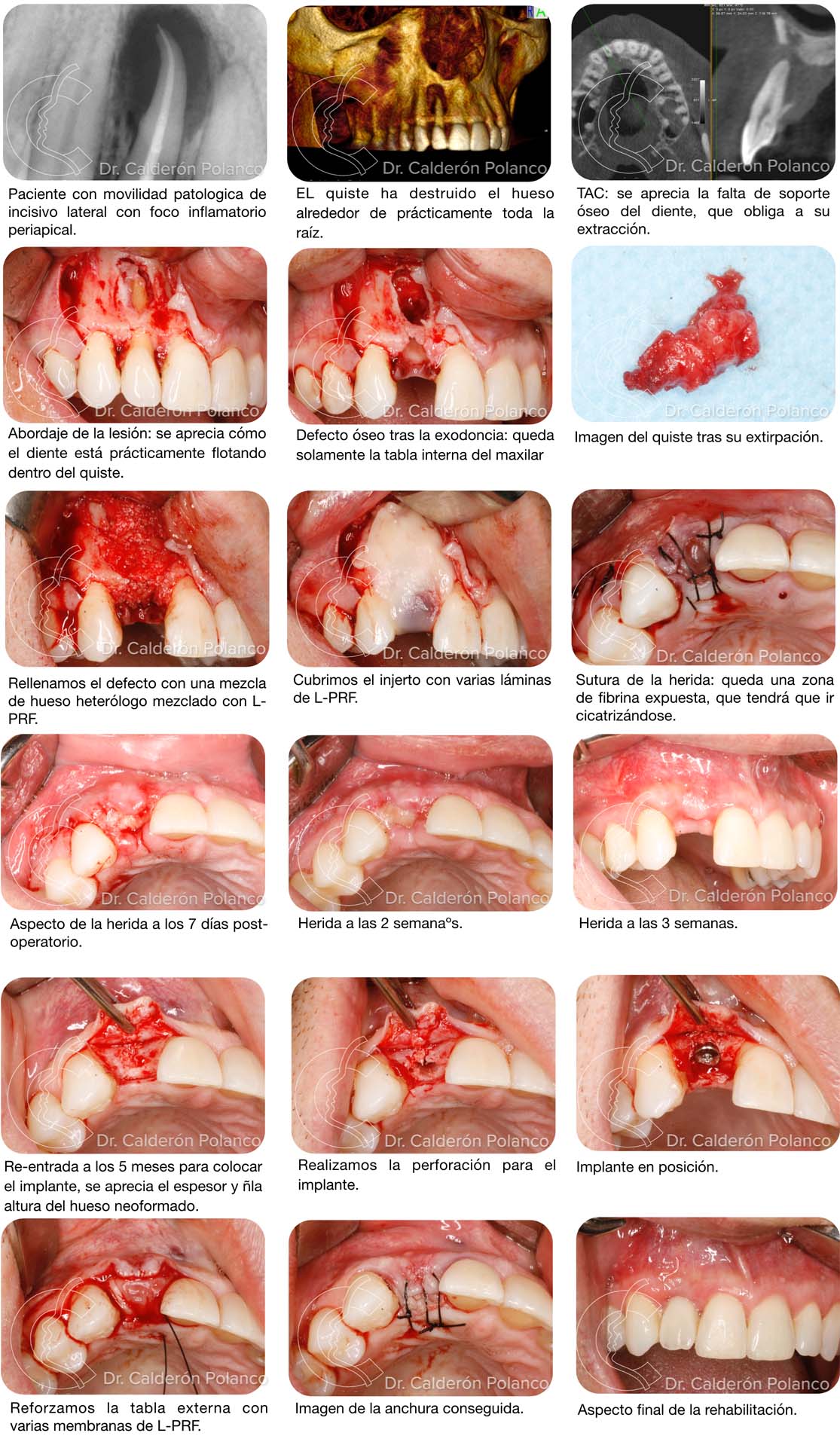
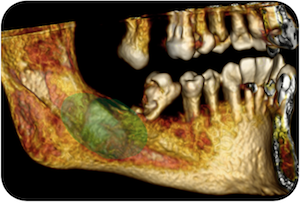
Caso 13 – Quiste en ángulo mandibular
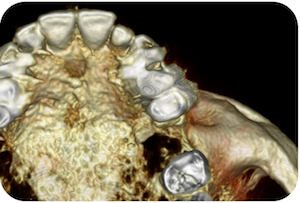
Caso 14 – Fístula Oro-Sinusal.
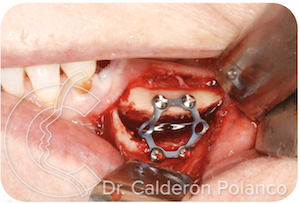
Caso 15 – Osteotomia de aumento óseo.
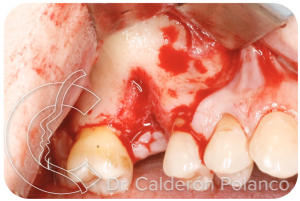
Caso 16: Defecto óseo del reborde alveolar»
Caso 13: Quiste en ángulo mandibular.
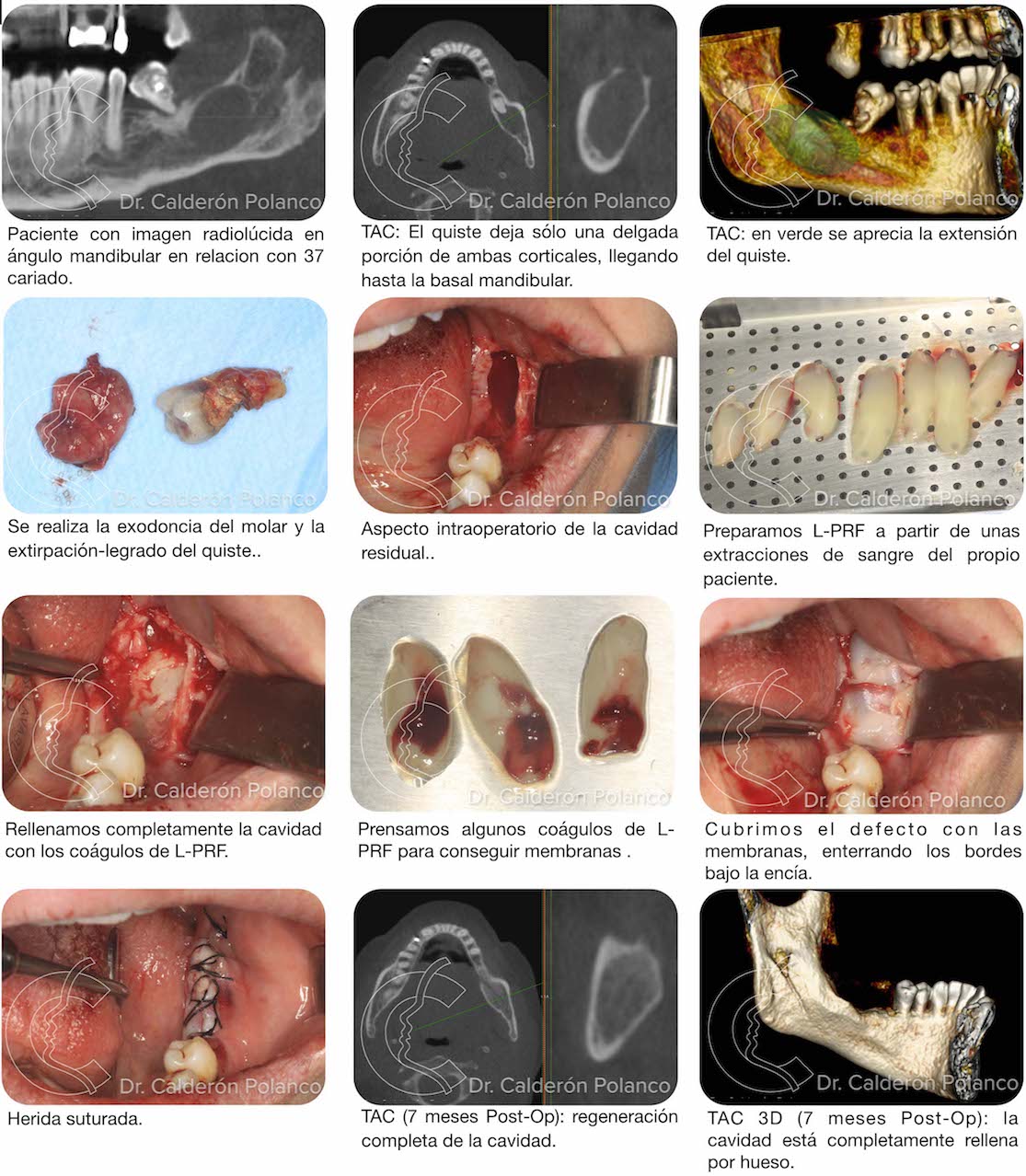
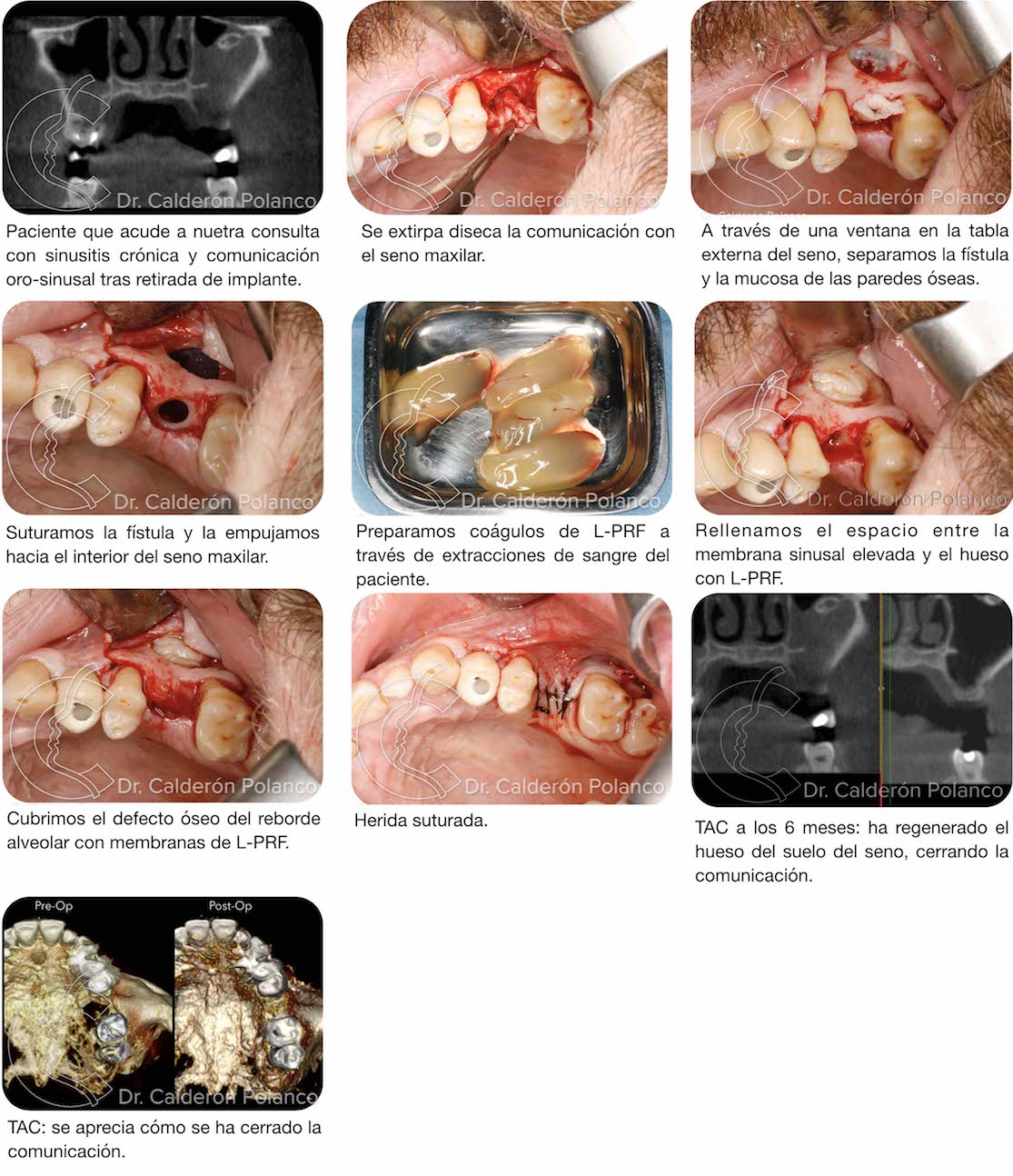
Caso 15: Osteotomia de aumento óseo.
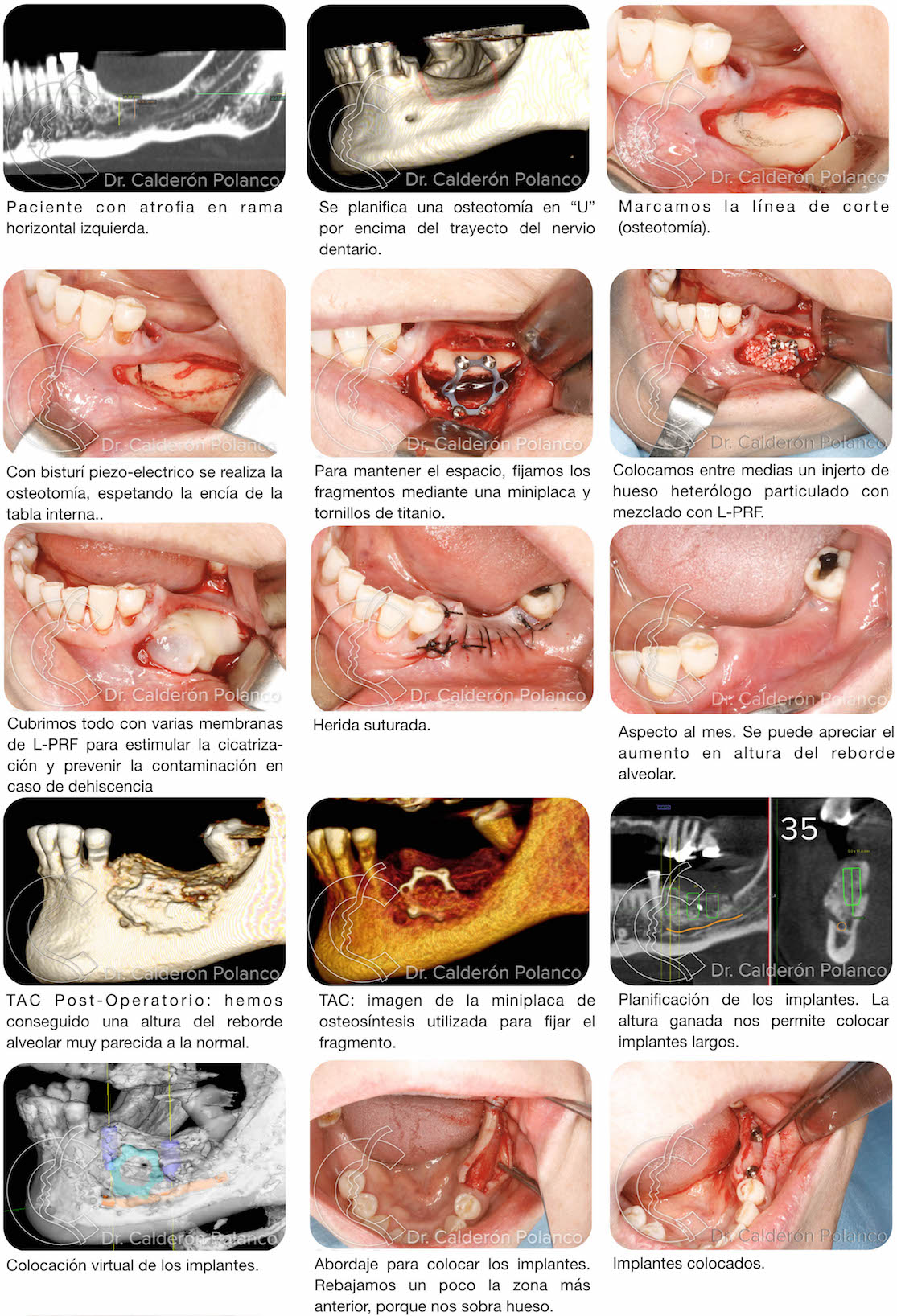
Caso 16: Defecto óseo del reborde alveolar
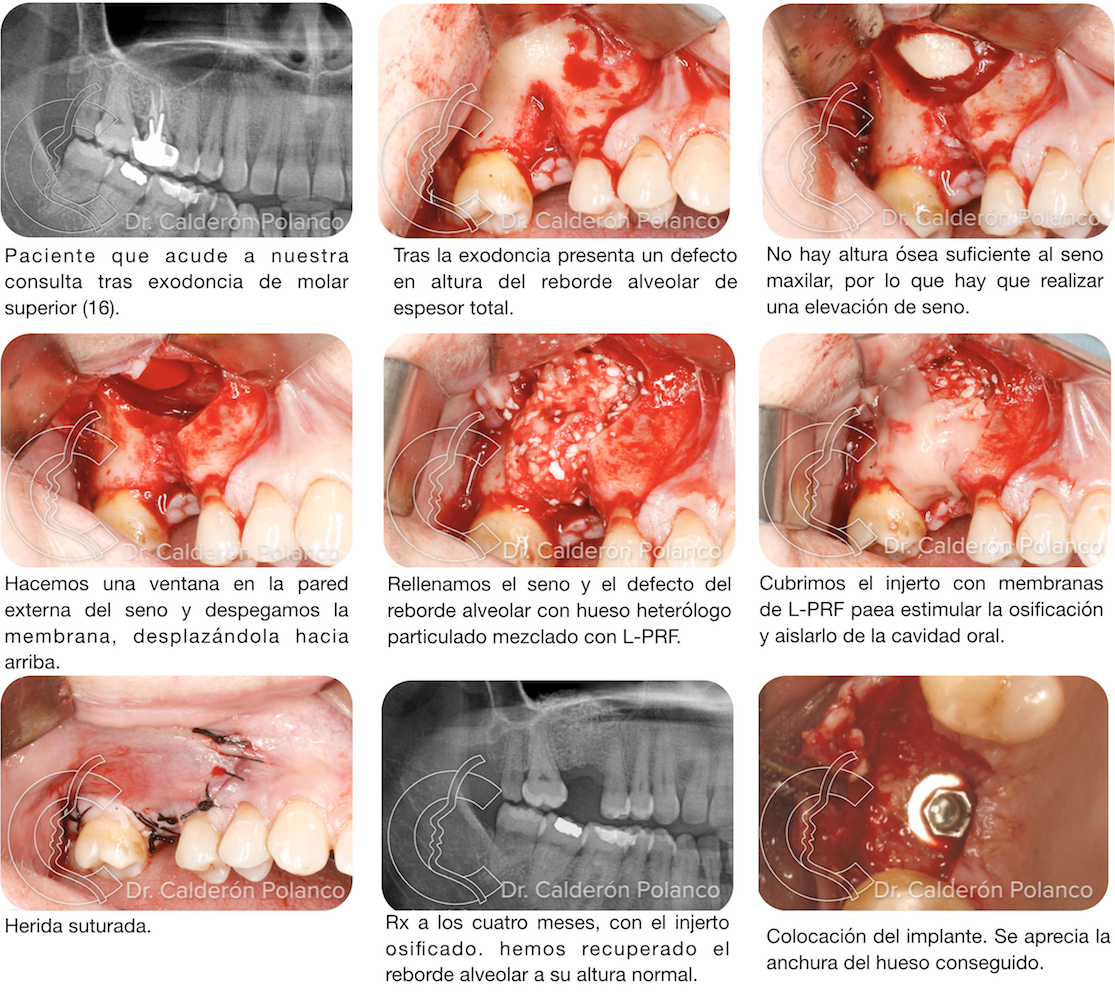
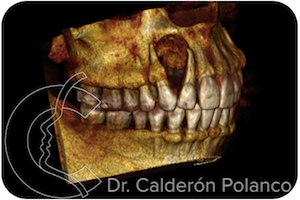
Caso 17 – Quiste en premaxila
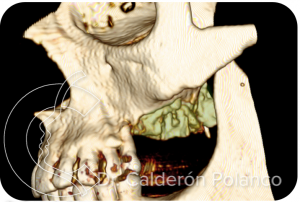
Caso 18 – Osteonecrosis por Bifosfonatos
Caso 19 –
Caso 20:
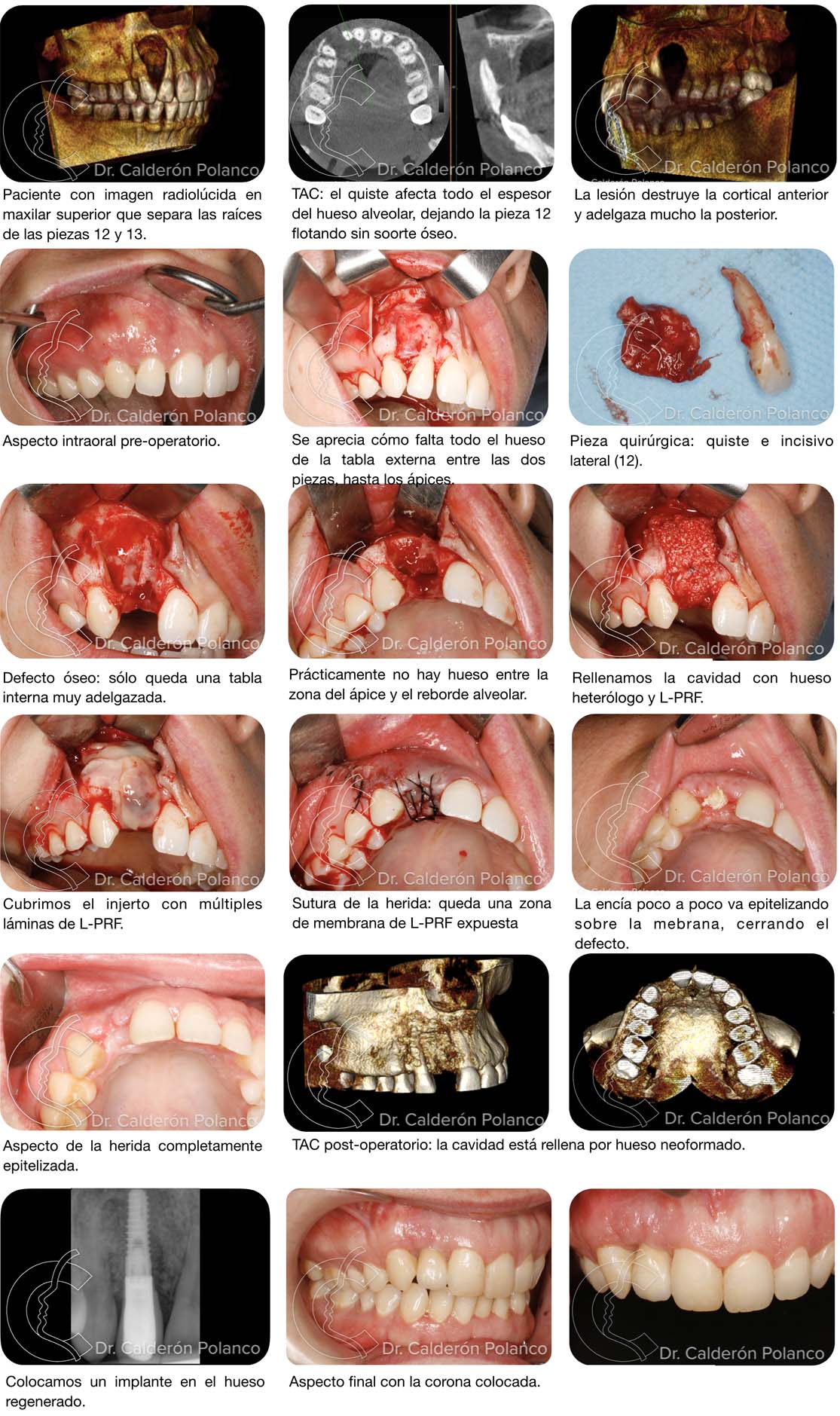
Caso 18: Osteonecrosis por Bifosfonatos
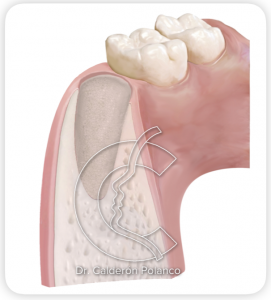
Después de una extracción dentaria se produce una reabsorción importante del hueso alveolar, tanto en altura como en anchura.
Estos cambios en el hueso alveolar post-extracción tendrán que tenerse en cuenta al planificar los implantes, sobre todo en las zonas de más riesgo.
La zona del alveolo con más riesgo de pérdida de hueso es la zona central, porque el hueso es más delgado que en las zonas laterales.
Estudios con TAC en alveolos post-extracción (Chappuis) han demostrado que se pierde mucho más altura cuando la pared ósea es delgada que cuando el hueso es grueso (atrofias de 7-8 mm frente a 1 mm).
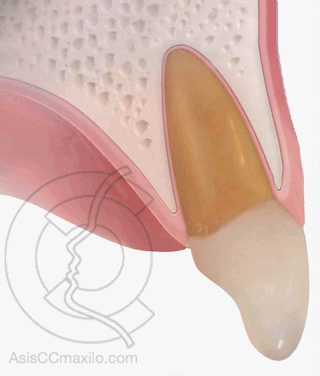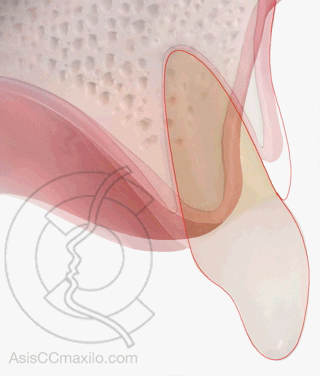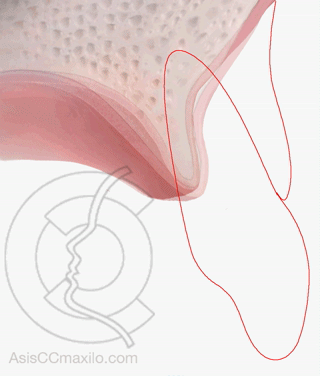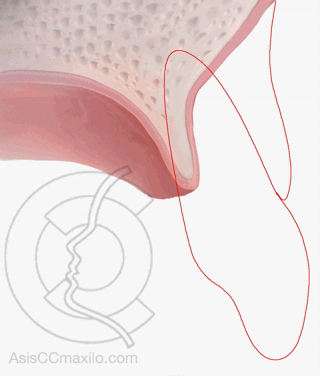
En la parte central del maxilar (zona estética), la tabla ósea externa es muy delgada, por lo que la mayoría de los implantes colocados en esta zona (incisivos y caninos), van a necesitar técnicas de regeneración ósea asociadas.
La utilización de L-PRF en los alveolos post-extracción reduce la atrofia ósea y mejora significativamente la cicatrización de las partes blandas.
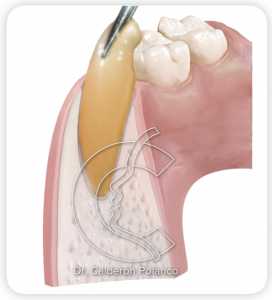
Es importante realizar una extracción dentaría atraumática, para conservar todo lo posible el hueso alveolar.
El siguiente paso después de legrar la cavidad y eliminar posibles restos de material inflamatorio, es ir rellenando el alveolo con varios coágulos de L-PRF.
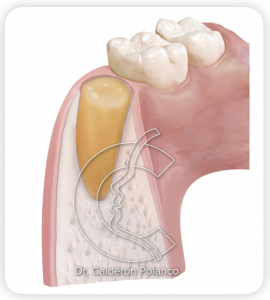
Si es posible, conviene aprovechar el exudado obtenido al comprimir el L-PRF para irrigar y limpiar el alveolo con una jeringa.
Después, hay que colocar varios coágulos dentro del alveolo, uno tras otro, comprimiendo con una gasa para compactarlos y eliminar el suero sobrante.
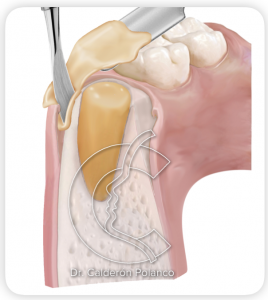
Hay que disecar un pequeño bolsillo subperióstico de unos 2-3 mm entre los bordes del hueso alveolar y la encía circundante.
Cubrimos el relleno del alveolo con, al menos, dos membranas de L-PRF, insertando los bordes de las membranas en el espacio creado entre el periostio y las paredes óseas.
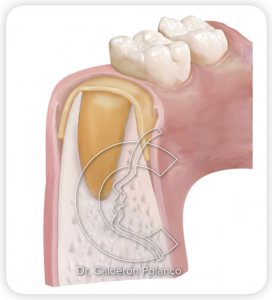
De esta forma, las membranas de L-PRF funcionan como un apósito biológico que sella el relleno del alveolo, separándolo de la cavidad oral, y forzamos al epitelio a crecer por encima de las membranas.
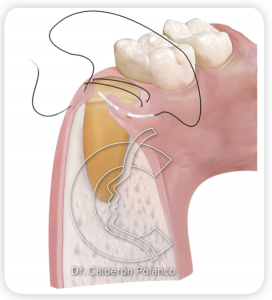
Suturamos la herida sin tensión, no con la intención de cerrar los bordes, sino de mantener el L-PRF en posición y que no se salga.
Hay que intentar apoyar las suturas en el hueso subyacente para minimizar la tensión sobre las partes blandas.
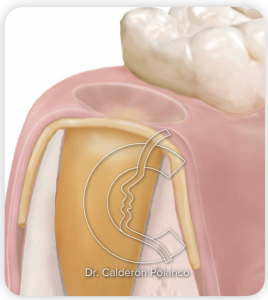
En los casos de extracciones dentarias, no hay encía suficiente para cerrar el defecto de forma primaria, por lo que buena parte de la membrana superficial de L-PRF quedará expuesta y en contacto con la cavidad oral.
El epitelio de la encía va a ir creciendo sobre al membrana, hasta cubrirla completamente
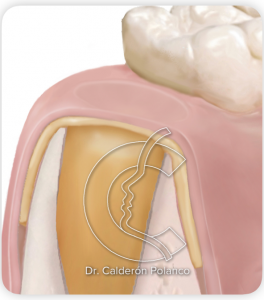
Durante un par de semanas, el tejido neoformado en muy tierno y puede deshacerse, por lo que es recomendable comer una dieta muy blanda y por el lado contrario. Una vez cicatrizada la encía, se puede comer normalmente.
En unos tres meses, el alveolo estará regenerado con tejido óseo y podremos colocar un implante.
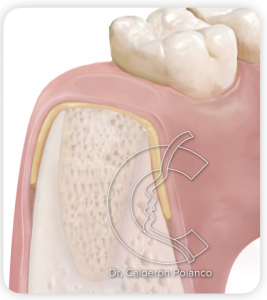
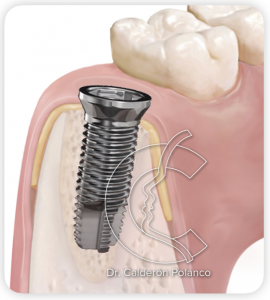
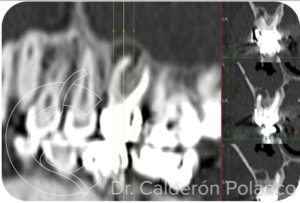
Paciente con quiste inflamatorio periapical por fracaso de endodoncia del 26.
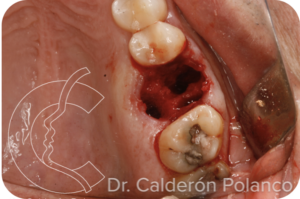
Se realiza la exodoncia de la pieza y legrado del material inflamatorio.
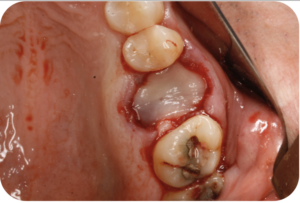
Rellenamos la cavidad alveolar con L-PRF y lo cubrimos con varias capas de membranas de L-PRF.
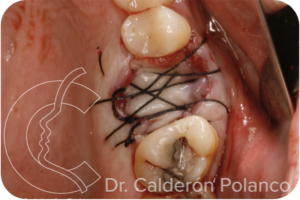
Suturamos la herida para mantener el relleno en posición y evitar que se salga el material.
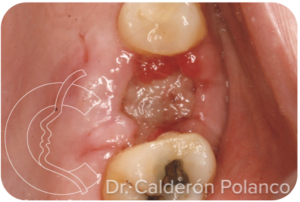
Aspecto de la herida al cabo de 1 semana. La encía va cicatrizando a partir de los bordes de la herida.
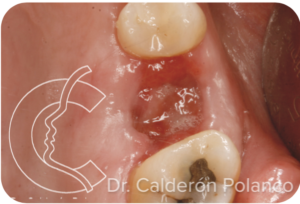
Aspecto de la herida a las 2 semanas. La membrana de L-PRF va cubriéndose por encía inmadura, todavía muy friable.
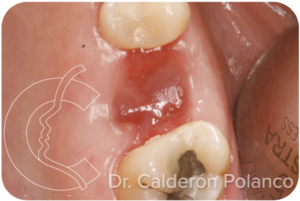
Alas 3 semanas la encía va madurando, cubriéndose de epitelio.
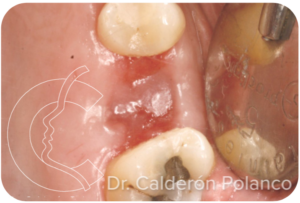
A las 4 semanas, casi toda la herida está cubierta por un epitelio todavía muy delgado.
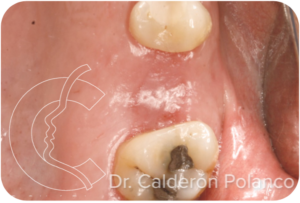
Al final, la encía adquiere un aspecto y consistencia normal.
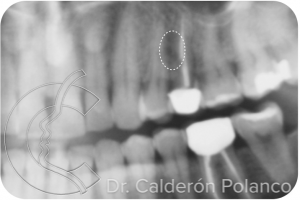
Paciente con fractura de raíz endodonciada con fístula por vestibular.
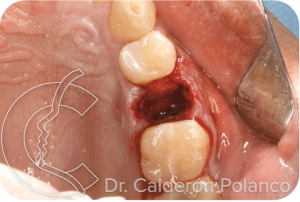
Se realiza la exodoncia de la pieza y legrado del material inflamatorio.
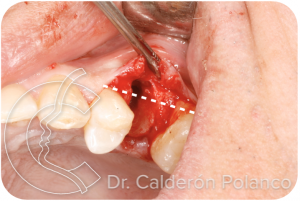
La fístula ha destruido la cortical externa del hueso alveolar.
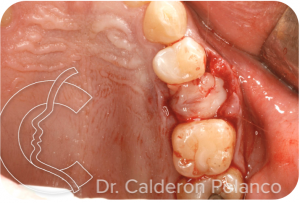
Rellenamos la cavidad alveolar con L-PRF y lo cubrimos con varias capas de membranas de L-PRF.
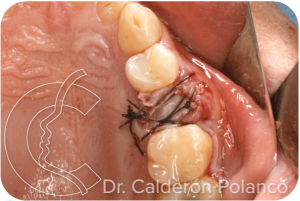
Suturamos la herida para mantener el relleno en posición y evitar que se salga el material.
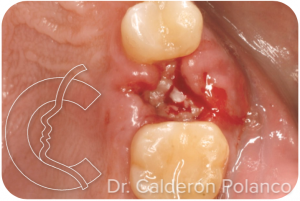
Aspecto de la herida a los 6 dias: el epitelio de la encía va creciendo sobre la membrana, cubriendo la herida.
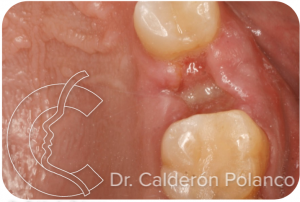
A los 11 dias la encía casi ha cubierto completamente la herida, queda una pequeña zona central expuesta.
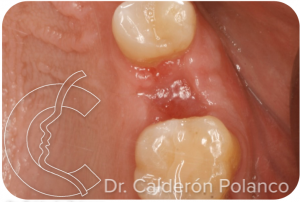
3 semanas: herida epitelizada, aunque todavía tierna.
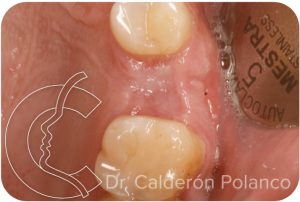
4 semanas: la membrana está cubierta por encía completamente normal.